Notice
 BOARD
BOARD
 Notice
Notice
김종승 교수팀, 약물전달과 흡수 직접 모니터링하는 약물전달 복합체 개발
김종승 교수팀 약물전달과 흡수를 직접 모니터링할 수 있는 약물전달 복합체 개발
부작용 낮추고 치료효과는 높인, 약물전달,흡수과정 확인하는 신개념 약물전달 복합체

▲ 이과대학 화학과 김종승 교수
국내 연구진이 정상세포가 아닌 암세포에만 약물을 정확히 전달하고, 그 전달과정까지 직접 모니터링할 수 있는 약물전달 복합체를 개발하여, 향후 신개념 암 진단과 치료법 개발에 가능성을 열었다.
고려대 김종승 교수(만49세)와 경희대 강철훈 교수(만51세)가 공동 주도하고, 고려대 이민희 박사가 참여한 이번 연구는 교육과학기술부와 한국연구재단이 추진하는 리더연구자지원사업(창의적 연구)의 지원으로 수행되었고, 연구결과는 화학분야의 권위 있는 학술지인 ‘미국화학회지(JACS)’지 8월호(8월 1일)에 표지논문과 주목할 논문(Spotlight)으로 게재됐다.
(논문명: Direct Fluorescence Monitoring of the Delivery and Cellular Uptake of a Cancer-Targeted RGD Peptide-Appended Naphthalimide Theragnostic Prodrug)

기존의 약물전달은 비선택적이었기 때문에 정상세포를 암세포로 만드는 등의 부작용이 있어, 암세포에만 선택적으로 약물을 전달하는 약물전달 시스템을 개발하고자 시도했다.
구체적으로 살펴보면, 기존의 약물전달 복합체는 암세포 내에서 구조나 위치를 고려하지 않고 무분별하게 약물을 전달하여 비효율적이었다. 또한 약물의 전달 여부를 확인할 수 없어 세포의 활성 또는 사멸 정도를 통해 간접적으로 유추해왔다. 아울러 기존의 약물전달 복합체가 고분자나 나노입자로 만들어져 잔여물이 그대로 남아 부작용을 일으키거나 분자가 커서 암세포까지 제대로 도달할 수 없는 등 단점이 있었다.
김종승 교수 연구팀은 암세포 지향 리간드*(RGD 펩타이드)와 효소활성 등을 이용한 약물전달 복합체를 유기화학합성으로 만들어 기존의 약물전달 복합체의 문제를 해결하는데 성공하였다.
*) 리간드(ligand) : 착물(錯物) 속에서 중심원자에 결합되어 있는 이온 또는 분자의 총칭으로, 배위자(配位子)라고도 함
특히 RGD* 펩티드는 종양과 관련된 혈관생성과 성장에 관여하는 단백질에 나타나며, 이 부분을 인지하는 수용체가 암세포 표면에 풍부하여 효과적인 암세포 표적지향체**로 작용한다.
*) RGD : 알기닌(Arginine), 글라이신(Glycine), 아스팔틱산(Aspartic acid)의 아미노산 서열을 일컬으며, 약자로 RGD라고 함
**) 표적지향체(guiding group) : 약물전달체계에서 표적 부위에 선택적으로 작용하여 약물의 흡수를 도와주는 물질로, 약물의 부작용을 최소화하고 효율을 증대시킴
김 교수팀은 우선 암세포에만 약물이 전달될 수 있도록 RGD 펩티드와 세포핵 내에 약물표적자를 가지고 있는 암세포 치료 약물(CPT 약물) 및 효소(-S-S, 다이설파이드)*를 연결하고, 약물이 나올 때 모니터링할 수 있도록 형광체(나프탈이미드 형광체)를 넣어 약물전달 복합체를 만들었다.
*) 다이설파이드(disulfide) : 시스틴(cystine)이 cysteine acid로 되는 산화 반응에서 생성되는 중간 생성물로, CPT 약물이 쉽게 끊겨 암세포를 치료할 수 있도록 돕는 역할을 함. 암세포엔 많고 정상세포엔 적음
이 약물전달 복합체는 RGD 펩티드가 있어 암세포에만 선택적으로 흡수될 뿐만 아니라, 약물표적자가 있는 핵주위로 약물을 정확히 전달할 수 있도록 하여 치료효과를 극대화했다.
또한 우수한 항암효과에도 불구하고 △강한 항암효과로 인한 부작용 △물에 대한 낮은 용해도 △혈액 속에서 쉽게 분해되는 문제점 등으로 실제 사용할 수 없었던 CPT(Camptothecin) 약물을 나프탈이미드 형광체와 연결한(-S-S 링커) 새로운 프로드러그* 형태로 개발함으로써, 표적부위에만 전달하여 부작용을 최소화하고 치료효과를 높였다.
*) 프로드러그(prodrug) : 약물에 특정 링커를 연결하여 약효를 억제하고 생체 내의 특정 효소반응에 의해 링커가 끊어졌을 때 그 약리활성이 회복되도록 하는 시스템
아울러 나프탈이미드 형광체가 있어 육안으로도 CPT가 암세포에만 흡수되어 효과적으로 암세포를 제거하는 모든 과정을 확인할 수 있는 것이 특징이다.
김종승 교수는 “이번 성과를 통해 약물을 정확히 전달하여 부작용을 최소화하면서도 치료효과를 극대화하였다. 또한 약물 전달과 흡수의 모든 과정을 육안으로 모니터링할 수 있게 됨으로써, 향후 다양한 질병에 맞춤형 약물을 개발하여 신개념 진단 및 치료법 개발에 기여할 수 있을 것으로 기대한다”고 연구의의를 밝혔다.
< 용 어 설 명 >
1. Journal of the American Chemical Society지
: 세계 최고권위의 학술지인 미국화학회지로 화학, 물리, 생물, 무기 등 다양한 과학 분야의 독창적이고 우수한 연구 결과를 주간으로 발간하는 세계적으로 영향력 있는 학술지.
2. RGD
: 알기닌 (Arginine), 글라이신(Glycine), 아스팔틱산(Aspartic acid)의 아미노산 서열을 일컬으며, 약자로 RGD라고 한다.
3. 표적지향체(guiding group)
: 표적지향체란 약물전달체계에서 표적 부위에 선택적으로 작용하여 약물의 흡수를 도와주는 물질로 약물의 부작용을 최소화하고 효율을 증대시킨다.
4. 프로드러그(prodrug)
: 약물에 특정 링커를 연결하여 약효를 억제하고 생체 내의 특정 효소반응에 의해 링커가 끊어졌을 때 그 약효가 회복되도록 하는 약물전달시스템
5. 소포체
: 세포 내 미세기관 중 하나로 핵 주변에 위치하며 합성된 단백질이나 중요 물질을 핵에 공급한다.
6. 테라그노시스(theragnosis)
: 치료(therapy)와 진단(diagnosis)의 합성 용어로 질병을 진단함과 동시에 치료가 가능한 첨단기술을 말한다.
< 사 진 설 명 >
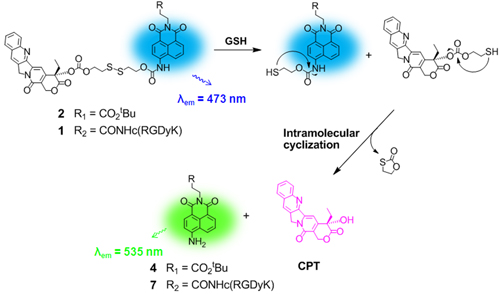
그림 1. 약물전달 및 모니터링이 가능한 표적화된 약물전달 복합체(1)와 GSH의 반응을 통한 형광 시그널 변화 및 활성 CPT약물의 방출 모식도
약물전달 복합체(1)는 αvβ3 인테그린과 관련된 암세포에 대한 표적지향체인 RGD펩타이드, 약물 방출시 모니터링이 가능한 시그널을 제공하는 형광체인 나프탈이미드, –S-S-에 연결되어 약리 활성이 없는 프로드러그 형태의 CPT약물로 구성된다. 약물전달 복합체(1) 내의 –S-S-는 GSH와 산화-환원 반응을 통해 끊어지고 535nm에서 새로운 형광 시그널과 동시에 활성 CPT약물을 방출한다.
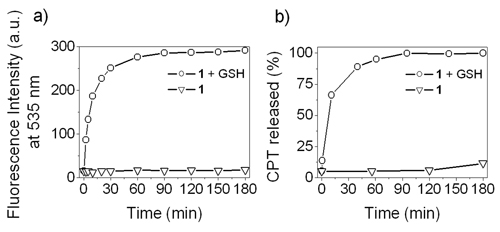
그림 2. 약물전달 복합체(1)와 GSH의 반응의 형광 시그널 변화와 CPT약물 방출의 상관관계
약물전달 복합체(1)와 GSH 물질의 반응에서 시간에 따라 증가하는 535nm의 형광 시그널(a)이 방출되는 활성 CPT약물 농도(b)와 비례함을 확인하였다.
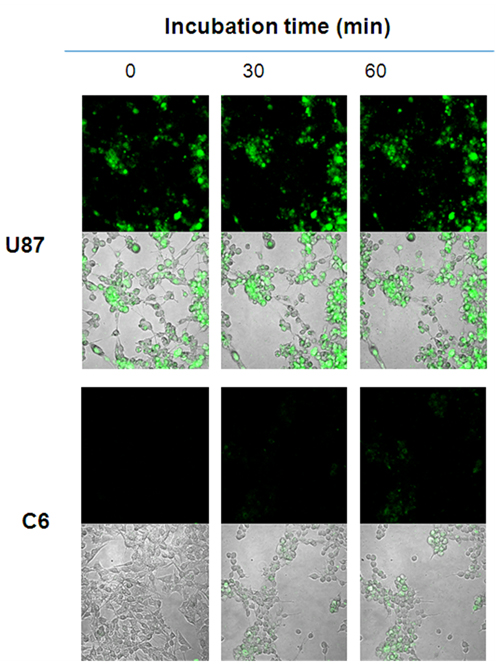
그림 3.
약물전달 복합체(1)의 표적세포로의 흡수 및 약물전달 형광이미징
αvβ3 인테그린 수용체의 고발현으로 알려진 U87세포와 저발현으로 알려진 C6세포 중에서 약물전달 복합체(1)의 RGD 펩타이드는 U87세포의 다량의 αvβ3 인테그린 수용체에 의해 인지되어 효과적으로 흡수되고 복합체(1)의 –S-S-와 세포 내의 GSH가 빠르게 반응해 535nm의 형광 시그널과 활성 CPT약물을 방출하는 것이 모니터링되었다.
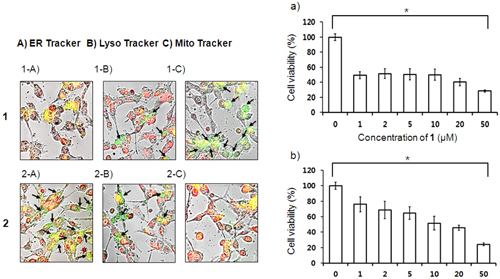
그림 4. 세포 내 소포체로의 복합체(1)의 약물전달 이미징 및 독성평가
약물전달 복합체(1)과 RGD 펩타이드가 없는 비교물질(2)를 U87셀에 넣고 세포 내 약물전달 위치를 확인하였고(왼쪽 세포 그림) 각각의 항암효과를 측정하였다(오른쪽 막대 그래프). 약물전달 복합체(1)는 소포체에 약물을 방출하고(1-A) 비교물질(2)은 미토콘드리아에 약물을 방출하는 것이 확인되었다(2-C). 또한 약물전달 복합체(1)는 1마이크로 몰에서 암세포의 50%를 사멸시켰고(오른쪽a) 비교물질(2)의 독성(오른쪽b)과 비교하였을 때 월등히 향상된 약리효과이다.




